Новые методы лечения рака крови (лейкемии, лейкоза)
Обновлено: 19.10.2023
Новые технологии лечения рака крови (лейкоза, лейкемии) включают в себя иммунотерапию, пересадку костного мозга, генотерапию, персонализированные вакцины. Ниже вы найдете каталог современных медицинских центров, в которых используются новейшие технологии лечения рака крови и новости о новых методиках.
2023. Gilead провалила испытание препарата против лейкемии стоимостью $4.9 млрд

Испытания препарата magrolimab для лечения острого миелоидного лейкоза (AML) остановлены фармакомпанией Gilead Sciences, т.к. он не смог улучшить выживаемость при этой болезни. Gilead купила этот препарат вместе со стартапом Forty Seven в 2020 году аж за $4.9 млрд, но похоже, деньги были потрачены впустую. Два месяца назад этот же препарат был признан бесперспективным для лечения миелодиспластического синдрома (MDS). И теперь единственная оставшаяся возможность для препарата доказать свою полезность - испытания его против множественной миеломы и диффузной В-клеточной лимфомы, которые находятся сейчас на 2 фазе. Препарат является антителом, нацеленным на рецептор CD47, который позволяет раковым клеткам избежать нападения иммунной системы.
2022. Merck купил перспективный препарат для лечения рака крови за $1,35 млрд
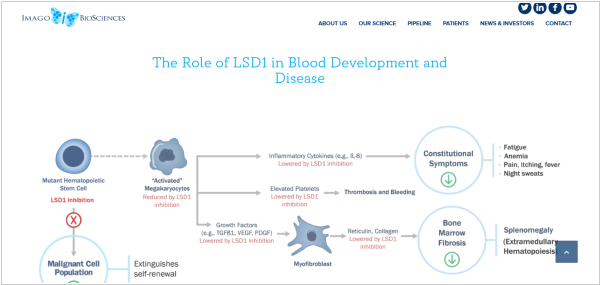
Американская фармакомпания Merck & Co (не путать с немецкой Merck) за $1,35 млрд купила стартап Imago BioSciences, который разработал препарат bomedemstat для лечения опасных для жизни заболеваний костного мозга. Imago BioSciences открыл молекулу-ингибитор лизин-специфической деметилазы 1 (LSD1) и довел ее до 2 фазы клинических испытаний, доказав, что ингибирование LSD1 уменьшает характерные симптомы миелопролиферативных новообразований (МПН), семейства раковых заболеваний костного мозга, которые могут трансформироваться в острый миелоидный лейкоз. Если все получится, Merck составит сильную конкуренцию существующим препаратам Jakafi (от Novartis) и Inrebic (от Bristol Myers).
2022. GlaxoSmithKline купила за $1.9 млрд препарат от миелофиброза

Миелофиброз - это заболевание, встречающееся при раке крови, при котором фиброзная ткань замещает кроветворные клетки в костном мозге. Существующие препараты против миелофиброза хорошо справляются с подавлением роста фиброзной ткани (за счет ингибирования фермента JAK), но приводят к малокровию - дефициту эритроцитов. Более 10 лет назад начались испытания препарата momelotinib, который должен решить эту проблему. И вот, похоже, что многолетняя надежда оправдается. Препарат практически прошел 3 фазу испытаний и бигфарма GlaxoSmithKline решила купить правообладателя - стартап Sierra Oncology за $1.9 млрд.
2021. В США одобрили первую генную терапию против множественной миеломы
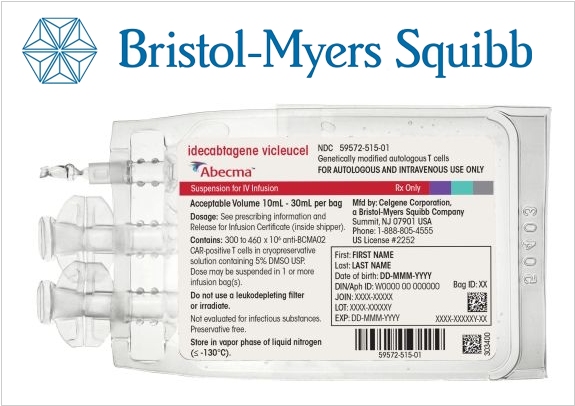
Множественная миелома - редкий тип рака крови, который до сих пор остается неизлечимым и после постановки диагноза наилучшим прогнозом для пациентов является долгая ремиссия. Новый препарат Abecma компании Bristol Myers, попробует изменить эту ситуацию. По результатам 3 фазы его клинических испытаний (в которых приняло участие 127 пациентов с рецидивирующей миеломой), более 70% пациентов ответили на лечение и около трети из них продемонстрировали полное исчезновение всех признаков рака. Abecma представляет собой Т-клеточную иммунотерапию (CAR-T). Процесс лечения основан на заборе и модификации Т-клеток пациента, которые после генетических изменений получают способность нацеливаться и уничтожать миеломные клетки. Однако, Abecma может вызывать серьезные побочные эффекты, поэтому ее назначение и лечение должно проходить под серьезным контролем.
2021. В Австралии создали перспективный препарат против острого миелоидного лейкоза
Команда ученых из Университета Монаша Австралийского центра заболеваний крови, под руководством профессора Эндрю Вея (на фото), представили результаты третьей фазы клинических исследований препарата CC-486. Несмотря на эффективность химиотерапии для лечения этого типа рака, в настоящее время большинство пожилых людей умирают в среднем в течение двух лет с момента постановки диагноза. Экспериментальное лечение увеличило выживаемость пациентов на 30%. Так, после приема CC-486 показатели выживаемости от момента ремиссии составили почти 25 месяцев, а в группе плацебо около 15 месяцев. Причем, испытания проводились среди пациентов старше 55 лет. Среди наиболее частых побочных эффектов ученые отметили осложнения на ЖКТ, которые не снижали качество жизни человека на протяжении всего периода наблюдений. Всего в исследовании приняли участие 472 пациента.
2020. Препарат Novartis улучшил результаты Bosulif для лечения лейкоза

Препарат для лечения хронического миелоидного лейкоза asciminib швейцарской компании Novartis в 3 фазе клинических испытаний показал лучшие результаты, чем популярный сейчас Bosulif компании Pfizer. Это оральный препарат, ингибитор тирозиназы (TKI), который подавляет рост раковых клеток. TKI-препараты (в т.ч. Bosulif и Gleevec) уже показывают отличные результаты в лечении лейкозов, обеспечивая как минимум 12 лет жизни пациентам. Но существует проблема возникновения резистентности к конкретному препарату, поэтому появление еще одного (тем более, с еще более высокой эффективностью) - это очень хорошая новость. Сертификация asciminib в США запланирована на 1 квартал 2021 года.
2020. Tafasitamab - новый препарат от рака крови - на подходе

Американская фармакомпания Incyte выкупает у немецкого биотек-стартапа MorphoSys права на препарат Tafasitamab почти за $2 млрд. Это препарат на основе антител для лечения B-клеточной лимфомы, хронического лимфоцитарного лейкоза (ХЛЛ) и В-клеточной неходжкинской лимфомы. Препарат усиливает работу иммунных B-клеток, которые цепляются к раковым клеткам и привлекают макрофаги для их уничтожения. На данный момент Tafasitamab проходит последнюю стадию клинических испытаний и его эффективность сравнима с более дорогой CAR-T терапией. Incyte надеется выпустить препарат в продажу уже в этом году.
2019. В России создали нейропроцессор для диагностики рака крови

Российский научно-технический центр Модуль разработал нейросетевое устройство, которое умеет анализировать микроснимки анализа крови и выявлять атипичные клетки, которые могут быть связаны со злокачественным заболеванием кроветворной системы. Нейросеть обучалась на массиве данных лаборатории патологической анатомии одной из малазийских клиник. Разработчики говорят, что точность диагноза от нейросети составляет 98%, а анализ проводится всего за несколько секунд. В перспективе нейросеть Модуля сможет определять раковые клетки по результатам биопсии других видов рака. Сейчас устройство готовят к сертификации FDA в США.
2017. В США одобрили вторую генную терапию для лечения рака крови

Американский регулятор FDA одобрил вторую генную терапию для борьбы с раком крови: препарат Yescarta (компании Kite Pharma). Он предназначен для лечения агрессивной лимфомы у взрослых. Первым одобренным антираковым генотерапевтическим препаратом стал Kymriah (компании Novartis). В Yescarta применяется та же технология (CAR-T), что и в первой генной терапии. Она редактирует иммунные Т-клетки так что они начинают атаковать раковые клетки. Стоит Yescarta немного дешевле - 373 тыс. долларов для одного пациента. Причем есть потенциал к снижению этой стоимости, т.к. в США - более 7 тысяч пациентов в год, которым подходит эта технология. А чем больше пациентом покупают препарат, тем дешевле он становится.
2017. Антираковая генотерапия CAR-T сертифицирована в США
Технология CAR-T и препарат Kymriah (Кимрия) швейцарской компании Novartis, которая уже доказала свою эффективность в лечении острого лимфобластного лейкоза, была сертифицирована американским регулятором FDA (что еще раз подтверждает ее действенность). Суть технологии в том, что врачи берут образец белых кровяных телец пациента, а потом в лаборатории перепрограммируют их в убийц опухолей. Затем клетки возвращают в тело, где они быстро группируются и уничтожают раковые клетки. Конечно, стоимость такого лечения - не всем по карману - $475,000. Правда, Novartis обещает вернуть деньги, если организм пациента не отвечает на лечение.
2017. Наночастицы перепрограммируют Т-клетки прямо в организме для борьбы с лейкемией
Традиционные подходы к иммунотерапии рака предполагают перепрограммирование иммунных клеток в пробирке и последующий их ввод в организм. А вот ученые из Онкологического исследовательского центра Фреда Хатчинсона разработали биоразлагаемые наночастицы, с помощью которых можно программировать Т-клетки прямо в организме. Чтобы Т-лимфоциты могли «убивать» раковые клетки, их модифицируют, оснащая искусственными химерными антигенными рецепторами (CAR). Наночастицы переносят гены, которые «программируют» CAR. Ученые снабдили наночастицы молекулами, благодаря чему те быстро достигают Т-клетки, которая их поглощает. Затем клетка направляет наночастицу к ядру, и она растворяется. Перепрограммированные клетки начинают работать в течение 24–48 часов и продолжают работать в течение пары недель. Во время эксперимента запрограммированные наночастицами Т-клетки замедлили прогрессирование лейкемии у мышей.
2017. Лекарство Гливек показывает отличные результаты в лечении лейкоза
Лекарство Гливек (Gleevec) компании Novartis изменило смысл диагноза «хронический миелоидный лейкоз» (ХМЛ). Таблетка, которую нужно принимать один раз в день помогает 83% пациентов с ХМЛ прожить 10 лет и более, пусть и с побочными эффектами, включающими характерную сыпь, тошноту и быструю утомляемость. До появления этого лекарства на рынке у пациентов с ХМЛ было три варианта действий: проходить курс химиотерапии токсичными препаратами, искать донора для пересадки костного мозга или просто умереть. Однако, стоимость годового курса терапии Гливеком - около 120 тыс. долларов США. У Гливека есть и дженерики - в них содержится то же действующее вещество, иматиниб (imatinib). Годовой курс иматиниба индийского производства стоит 400 долларов, а канадского - 8800 долларов США.
2016. Персонализированная вакцина остановила рак крови

Медицинский центр Beth Israel Deaconess, расположенный в Бостоне, провел успешные клинические испытания новой вакцины, изготавливаемой из собственных клеток пациента, которая предназначена для лечения острого миелоидного лейкоза. Вакцина использует технологию иммунотерапии, т.е. стимулирует собственные имунные Т-клетки для уничтожения опухоли. Испытания начались 4 года назад, когда 17 пациентам со средним возрастом 63 года начали вводить вакцину после сеансов химиотерапии. В результате 12 из них до сих пор показывают ремиссию. На фото - руководитель проекта - Дэвид Авиган.
2016. Технология Cellectis вылечила уже второго ребенка от лейкемии

Франко-американская компания Cellectis, похоже, заняла лидирующую позицию на многообещающем рынке иммунотерапии рака. В конце прошлого года ее технология TALEN (основанная на методе CAR-T) помогла вылечить годовалую девочку от лейкемии, а недавно они объявили о второй успешной операции, проведенной в том же лондонском госпитале. Смысл технологии в том, что ДНК иммунных клеток (Т-лимфоцитов) модифицируется в пробирке, а затем они вводятся в организм, где уничтожают поврежденные при лейкемии кровяные клетки. Есть еще три перспективных стартапа, разрабатывающих подобные технологии (Novartis, Juno Therapeutics и Kite Pharma). Но отличие технологии Cellectis в том, что она использует донорские Т-клетки, т.е. потенциально может создать универсальный и дешевый препарат, который можно быстро ввести любому пациенту.
2015. Генная инженерия и иммунотрапия спасли девочку от лейкемии
В Лондонской больнице Грейт-Ормонд-Стрит врачи использовали уникальный метод CAR-T для лечения лейкемии (рака крови) у маленькой девочки Лейлы (1 год). Химиотерапия и пересадка костного мозга ей не помогли, поэтому медики решились испробовать новый вид иммунотерапии. Они взяли иммунные клетки донора, генетически-модицифировали их так чтобы они распознавали и уничтожали раковые клетки и при этом сами не воспринимались иммунной системой, как чужеродные, и ввели их в организм девочки. Через три месяца Лейле снова пересадили костный мозг: здоровые иммунные клетки распознали генно-модифицированные клетки как чужеродные и уничтожили их. Таким образом, сейчас в организме девочки не осталось генетически модифицированных клеток. Пока о полном излечении Лейлы говорить рано, но она жива и хорошо себя чувствует. Полноценные клинические испытания этой технологии начнутся в 2016 году. Технология разработана французской биотехнологической компанией Cellectis.
2014. Создан искусственный костный мозг для выращивания стволовых клеток крови
Все клетки крови (эритроциты, лейкоциты...) формируются из так называемых гемопоэтических стволовых клеток, которые, содержатся в костном мозге человека. И иногда человеку требуется замена этих стволовых клеток. Например, при лейкемии, когда собственные стволовые клетки превращаются в раковые. Или после лучевой терапии, когда собственные стволовые клетки погибают. В таких случаях проводят трансплантацию костного мозга, и это очень-очень дорогая операция, в основном из-за сложности поиска совместимого донора. В России с этим делом - вообще комедия. Вот было бы здорово, если б можно было взять у человека чуть-чуть стволовых клеток крови, размножить их в лаборатории, а потом ввести обратно в костный мозг. Именно над такой идеей работают ученые из нескольких ведущих научных центров Германии. И у них уже кое-что получилось. Они создали искусственную пористую структуру, имитирующую губчатое вещество кости в области кроветворного костного мозга. ***
2013. В Ханты-Мансийске проводят трансплантацию стволовых клеток при лечении рака крови
Югорский научно-исследовательский институт клеточных технологий, созданный четыре года назад, вроде-как успешно применяет свою технологию лечения рака крови с помощью стволовых клеток. На базе Сургутской ОКБ они провели уже 34 трансплантации стволовых клеток, и говорят, что все пациенты до сих пор живы. Кроветворные стволовые клетки НИИ получает от доноров (из костного мозга и пуповинной крови), проводят ДНК анализ (для определения совместимости) и хранит этот материал в своем криобанке. Затем стволовые клетки добавляют в кровь пациента каким-то уникальным методом. По словам Сергея Щукина, заместителя директора Департамента здравоохранения Югры, стоимость пересадки стволовых клеток на западе - порядка 420 тысяч долларов. А у нас по стране, хотя такие операции - редкость, но делаются они бесплатно, за счет средств бюджета.