Новости Медицины 2.0
08.07.2025
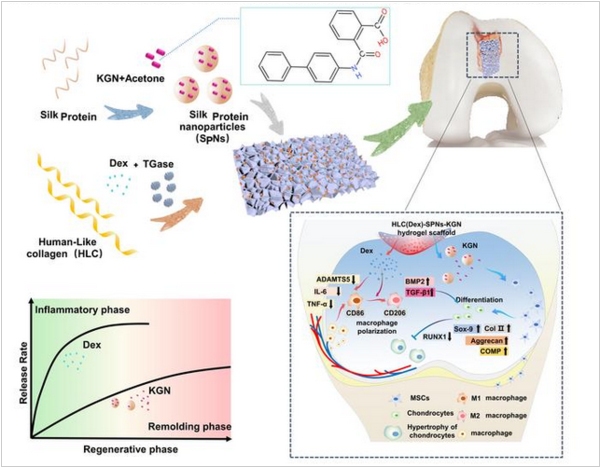
Команда ученых из Северо-Западного университета Китая разработали гидрогель для восстановления хряща при остеоартрите. Он снижает уровень воспаления в ткани и обеспечивает благоприятную среду для естественного восстановления. Поэтапное восстановление обеспечивается за счет медленного высвобождения препаратов: сначала действуют противовоспалительные, а затем медленно проникают соединения, которые стимулируют мезенхимальные стволовые клетки дифференцироваться в хондроциты, а также поддерживают их функцию в долгосрочной перспективе. Эксперименты на моделях кроликов показали полное восстановление дефектов хрящевой ткани. Теперь ученые совершенствуют гидрогель для будущего тестирования в рамках клинических экспериментов. Помимо восстановления хряща технологию планируют адаптировать для регенерации дефектов сухожилий и костей.
01.07.2025
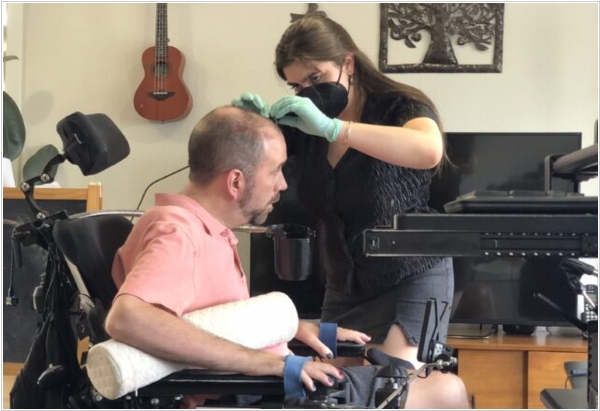
Группа ученых из Калифорнийского университета (UC) под руководством Майтрейи Вайрагкар, создали (и установили первому пациенту) гибкий речевой нейропротез, который позволяет пациенту с параличом говорить довольно бегло, управляя собственной интонацией, и быть более выразительным (по крайней мере по сравнению со Стивенов Хокингом). В отличии от других протезов (в т.ч. Neuralink), этот переводит считываемые с нейронов импульсы не в слова, а в звуки. Это получается значительно быстрее, т.к. при переводе в слова - система ждет окончания предложения и только потом определяется с набором слов для воспроизведения. Всего в системе используется 256 электродов, которые вживляются в вентральную часть прецентральной извилины. Сигналы нейронной активности отправляются в ИИ-декодер — который угадывает речевые характеристики, такие как высота тона или голос.
17.06.2025
Changsong Qi, профессор Пекинского Онкологического центра, представил результаты 2 фазы клинических испытаний терапии Satri-cel для лечения рака желудка. Лечение представляет собой разновидность CAR-T-клеточной иммунотерапии, при которой собственные иммунные клетки пациента (Т-клетки) извлекаются, модифицируются для более эффективного распознавания раковых клеток и затем возвращаются в организм. Препарат Satri-cel нацелен на белок CLDN18.2, который используют некоторые опухоли для роста. Это позволяет иммунным клеткам более точно атаковать раковые клетки, не затрагивая здоровые ткани. В 2-летнем испытании участвовали 156 пациентов с раком желудка или гастроэзофагеального перехода, которым не помогли как минимум два предыдущих лечения. У пациентов, получавших satri-cel, продолжительность жизни в среднем увеличилась на 40% по сравнению с контрольной группой, получавшей стандартную терапию. Это значительное улучшение, которое дает надежду пациентам с этим тяжелым заболеванием.
10.06.2025
Команда ученых из Медицинского университета Нара под руководством профессора Хироми Сакая, начала 1 фазу клинических испытаний искусственной крови - перспективной разработки, которая может изменить подход к переливанию крови по всему миру. В ходе испытаний 16 здоровым добровольцам ввели от 100 до 400 миллилитров искусственной крови, и если ученые не зафиксируют побочных эффектов, исследование продолжится, сосредоточившись на эффективности и безопасности нового продукта. Искусственная кровь, над которой работает команда Сакая, предназначена для универсального применения — ее можно переливать абсолютно всем, независимо от группы крови и резус-фактора, при этом срок хранения разработанной учеными жидкости составляет до двух лет. В качестве переносчика кислорода в ней используется гемоглобин, извлекаемый из просроченной и подлежащей утилизации донорской крови. Его помещают в липидную оболочку и формируют частицы, которые имитируют работу эритроцитов, но при этом не содержат антигенов группы крови и не несут риска передачи вирусов.
03.06.2025
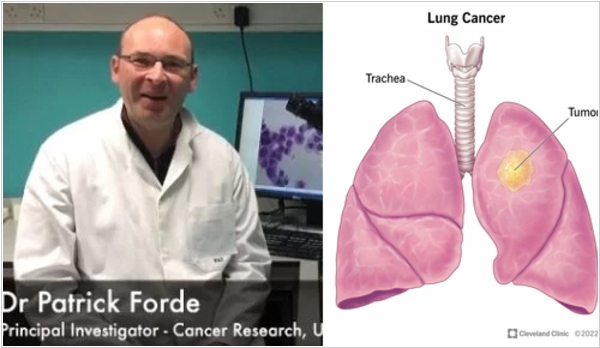
Команда ученых из медицинской школы Тринити-колледжа (Ирландия) под руководством Патрика Форд завершили 3 фазу клинических испытаний иммунотерапии на базе ниволумаба, экспериментального препарата для лечения лимфомы и опухолей кожи, для борьбы с самыми тяжелыми формами немелкоклеточного рака легких. Ниволумаб представляет собой синтетическое антитело, которое блокирует работу рецептора PD-1, своеобразного "тормоза" активности некоторых типов иммунных клеток. Результаты показали, что долгосрочная вероятность выживания пациентов повышалась примерно на 10% при приеме комбинированной химиотерапии и иммунотерапии по сравнению с одной химиотерапией (65% против 55%). При этом почти все пациенты (95%), у которых все следы опухоли полностью исчезли из организма после операции, прожили как минимум пять лет после начала эксперимента и не умерли от рецидива рака легких.
27.05.2025
Хирурги медицинского центра Рональда Рейгана при Калифорнийском университете в Лос-Анджелесе успешно провели первую в мире пересадку мочевого пузыря человеку. 41-летний пациент до этого 7 лет жил с мочевым пузырем размером с грецкий орех (из-за редкой формы рака мочевого пузыря его орган практически полностью удалили). Попытки пересадить мочевой пузырь от донора долго считались невозможными. Орган расположен глубоко между костями таза, куда сложно добраться хирургическими инструментами, и окружен сложной сетью сосудов. Его извлечение требует ювелирной точности, чтобы сохранить кровоснабжение для последующей трансплантации. Донорский мочевой пузырь для Ларрайнсара подобрали через организацию OneLegacy — крупнейший в США центр по заготовке органов.
19.05.2025
Препарат Olaparib, который принадлежит британской компании AstraZeneca, применяется для лечения рака еще с 2014 года. Однако, новый протокол его использования совместно с химиотерапией для лечения рака груди (перед операцией) - позволил добиться значительно лучших результатов. Исследование было проведено командой из Кембриджского университета. В нем приняли участие пациенты с раком груди на ранней стадии с унаследованными мутациями генов BRCA1 и BRCA2. В результате, из 39 участников исследования только у одного был рецидив через три года после операции. При этом все 100% показали трехлетнюю выживаемость. Для сравнения в контрольной группе (химиотерапия + операция по удалению опухоли) выживаемость составила только 88%. Новый протокол применения препарата более эффективен, а также более экономичен, поскольку лечение короткое. Если вторая фаза исследований с участием большей выборки пациентов покажет аналогичный результат, то клинические рекомендации будут скорректированы.
12.05.2025
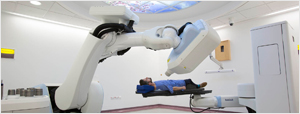
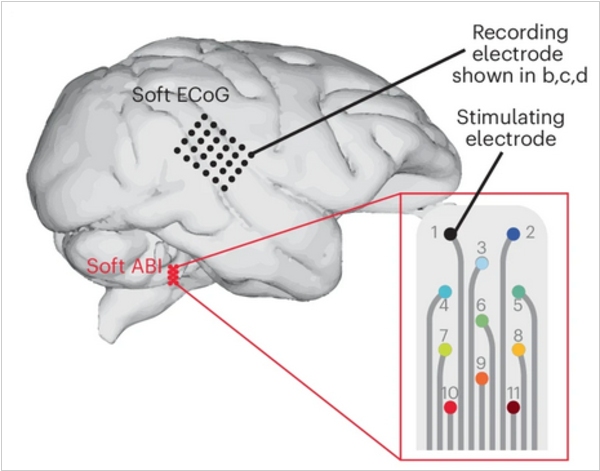
Исследователи из Федеральной политехнической школы Лозанны (EPFL) разработали набор из гибких электродов и электроники, который можно подключать к той части мозга, которая связана с восприятием звуков. Это перспективное решение для тех пациентов, которым по медицинским причинам нельзя устанавливать кохлеарный имплант (который передает сигналы при помощи электродов в улитку внутреннего уха, где они считываются слуховыми нейронами). Работа новой системы восстановления слуха была успешно проверена на обезьянах. Наблюдения показали, что животные хорошо "слышали" отправляемые на нейроимплант звуки и реагировали на них, и при этом они не испытывали дискомфорта при длительной имплантации электродов. Этот успех, как надеются ученые, позволит уже в ближайшее время приступить к проверке данной технологии в опытах на добровольцах.
05.05.2025
У детей с РАС часто присутствуют нарушения в работе желудочно-кишечного тракта. Команда исследователей из Университета штата Аризоны решила изучить потенциал трансплантации микробиоты в качестве лечения РАС и провела исследование, в котором приняли участие 18 детей. Образцы микробиоты вводились участникам в течение 7-8 недель, и уже на первом этапе было отмечено сокращение поведенческих симптомов. Через 2 года после трансплантации тяжелая форма РАС осталась только у 17% детей, а в среднем симптомы аутизма снизились на 45%. В 2022 году ученые запатентовали конкретную бактериальную формулу и создали компанию Gut-Brain Axis Therapeutics, которая будет заниматься дальнейшей работой. В настоящее время готовится финальная фаза клинических исследований, которая должна предоставить необходимые доказательства безопасности и эффективности для одобрения терапии.
18.04.2025
Болезнь Паркинсона связана с гибелью нейронов, вырабатывающих дофамин, и сопровождается тремором, скованностью и замедлением движений. Лекарства, полностью излечивающего болезнь, пока нет. Новое исследование, которое провели в США и Канаде - дает надежду на его появление. В нем участвовали 12 пациентов. Ученые вырастили нейрональные клетки из эмбриональных стволовых клеток и ввели их в область мозга, которая участвует в моторных функциях и нейроны в которой часто погибают при болезни Паркинсона. В течение года пациенты принимали иммуносупрессоры для предотвращения отторжения. Сканирование мозга показало увеличение выработки дофамина, при этом улучшение сохранялось в течение 18 месяцев после процедуры. Несмотря на обнадеживающие результаты, эксперты подчеркивают необходимость более масштабных исследований для подтверждения эффективности методов.